摘要
本研究有助于当前世界范围内旨在用氢取代炼钢过程中的化石碳的活动,从而大大减少温室气体排放。在700 ~ 1100℃的温度范围内,在纯氢气和氢、氩的混合物中等温还原由氧化铁颗粒制成的压坯。使用热重分析(TG)技术连续记录了还原过程中产生的总重量损失。结果表明,温度对转化率和还原率有相当大的影响。在一定温度下,随着还原气体中H2含量的增加,还原速率加快。结果表明,当H2含量大于80%时,对还原行为没有影响。样品的还原反应是由赤铁矿逐步还原为金属铁的。应用数学模型和还原样品的形态结构推导了还原动力学和机理,并与表观活化能(Ea)值进行了关联。初期、中期和末期的Ea值分别为16.36、29.24和49.35 kJ/mol。还原过程的前期由化学反应控制,后期由气体扩散控制。在中间阶段,还原过程受气体扩散和化学反应的混合机制控制。
图形抽象
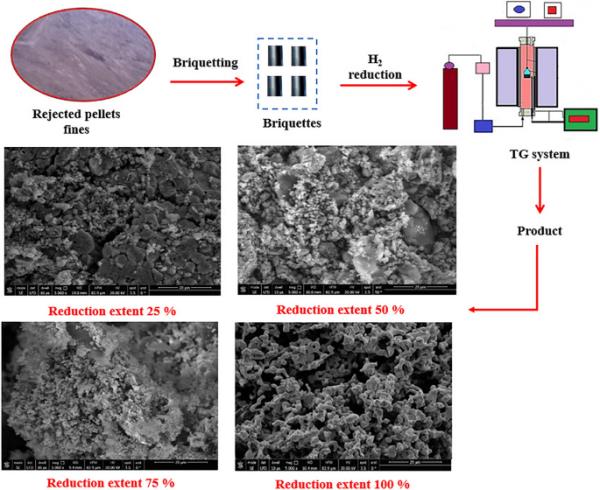
介绍
二氧化碳排放是目前最严重的环境挑战之一,其后果之一就是全球变暖。钢铁工业约占世界二氧化碳排放总量的7%[1]。平均每生产一吨粗钢排放约1.9吨二氧化碳。因此,钢铁行业正在探索减少二氧化碳排放的新方法,同时也使钢铁制造过程更加环保和经济可行[2]。钢铁制造公司正在为自己设定一个目标,成为一个低碳或碳中和的行业。使用氢作为还原剂[3,4,5,6],碳捕获储存和利用[7,8,9,10]生物质作为还原剂[11,12]被认为是减少化石燃料CO2排放的可能途径。氢是一种高效还原剂和清洁能源,是21世纪很有前途的能源介质。它的扩散和还原能力使其成为改善氧化铁还原的热力学和动力学条件的理想选择,从而提高还原速率。此外,H2较低的粘度和体积降低了气体的密度和粘度,从而更好地利用了热能。探索减少二氧化碳排放的方法之一是使用绿色氢生产直接还原铁(DRI)。此外,直接向高炉喷氢是实现低碳炼铁和绿色可持续发展的关键一步。然而,用氢替代化石燃料存在一些挑战,包括成本、运输和储存。此外,用氢还原铁矿石是一个吸热过程,需要较高的能耗[13,14,15]。
国际能源署(IEA)提供了一些关于直接还原铁(DRI)生产到2070年可持续发展情景的重要数据[16];其中一些数据摘编在表1中。
可以看出,100% H2技术生产DRI有望成为实现低碳或碳中性钢铁行业目标的主要关键参与者。
一氧化碳和氢都有还原氧化铁的能力,其中氢还原产生的是水蒸气而不是二氧化碳。到目前为止,在直接还原(DR)装置中,氧化铁的还原是通过重整天然气来实现H2和CO的结合。因此,看起来未来DR工厂使用的唯一还原剂将是氢气,经过一些修改和技术和经济方面的考虑。此外,从生物质等可再生资源中生产氢气使该过程更加环保。有鉴于此,氢基铁矿石还原技术最近引起了人们的极大兴趣[17,18]。
目前,研究人员正在研究在炼铁中利用氢气而不是冶金焦炭。三家瑞典公司正在研究氢气在钢铁制造过程中的利用。这个过程被称为氢突破炼铁技术(HYBRIT)。该方法的目标是用氢气完全替代冶金焦[19,20]。随着炼钢过程对DRI的需求日益增长,人们越来越重视推进DR工艺的研究[21]。例如,研究氧化铁在H2、CO和CO/H2混合气体中的还原动力学。
Pritesh Garg等[22]在1023 ~ 1373 K的温度范围内,使用不同的H2/H2O气体混合物对氧化铁颗粒粉进行了还原研究。他们使用了带有热重分析(TGA)装置的定量蒸汽发生器来控制还原性气体混合物中H2O的使用。研究分析了不同摩尔分数H2和H2O对Fe2O3整体还原动力学的影响。结果表明,当水摩尔分数较低时,反应受第一、第二阶段的化学反应控制。然而,当H2O摩尔分数较高(20%)时,反应在第二阶段结束时变为扩散控制。第二阶段的表观活化能随着还原气中H2O含量的增加而增加。将H2摩尔分数控制在50%和90%,进行了逐步还原实验,使Fe2O3-Fe反应解耦。
Daniel等[23]研究了873 ~ 1073 K范围内铁矿粉氢还原动力学。他们确定还原动力学不能用一个简单的气固反应模型来表示。速率控制机制取决于温度和还原程度。还原反应分为Fe2O3-Fe3O4、Fe3O4-FeO和FeO-Fe三个步骤。计算得到Fe2O3-Fe3O4、Fe3O4 - FeO、FeO - Fe的活化能Ea分别为11 ~ 55,23 ~ 55,23 ~ 42kj /mol。
Piotrowski等[24]研究了气体成分对氢气氛中氧化铁还原动力学的影响。他们证明了还原速率随着温度的升高和混合气体中H2含量的增加而增加。结果表明,当表面形成一薄层磁铁矿和浮士体时,控制还原过程的机制由表面控制转变为气体扩散控制。
在700 ~ 1100℃范围内研究了H2-H2O对铁矿石球团等温还原的影响[25]。比较了由CO-CO2-H2-H2O-N2组成的还原性气体混合物与单纯含有CO-CO2-N2的还原性气体混合物的性能。结果表明,在两种还原气氛中,提高还原温度会导致更大的还原水平。随着温度的升高,孔隙率和比表面积也增加,从而改善了还原过程。还原气体H2和H2O增加了还原球团的孔隙率和表面积,从而提高了还原效率。然而,在800°C和900°C时,水蒸气含量超过2%的气体成分的还原性能并没有明显优于co - co2 - n2还原气氛,因为水蒸气可能阻碍了浮氏体的活性位点
Metolina等[26]研究了工业赤铁矿球团在氢气气氛下的还原,以评价工艺因素对整体还原反应的影响。研究结果表明,颗粒大小和温度之间存在显著的相互作用,这对还原行为有重要影响。结果表明,颗粒尺寸和温度对还原过程有重要影响,两者之间存在显著的相互作用。随着温度的升高,颗粒的尺寸变小,还原的速度急剧增加。相比之下,在本次调查覆盖的区域内,孔隙度对该过程没有显著影响。颗粒体积在600至1000°C的温度范围内几乎保持不变。颗粒体积在1000时显著增加,这与裂缝的发展有关。
Yong Lee等[27]研究了不同升温速率下Fe2O3纳米粉体在H2气体中的非等温还原动力学。他们得出结论,在还原反应中,相变的顺序是Fe2O3变为Fe3O4, Fe3O4变为Fe。基于非等温(TG)测量,采用Kissinger-Akahira-Sunose (KAS)模式测定表观活化能Ea。在还原阶段(从Fe3O4到Fe),氧化物颗粒的烧结减慢了反应速率,从而使活化能突然升高。随着金属铁晶粒的增大,生成的铁颗粒促进周围氧化颗粒还原的催化作用是导致反应速率加快的原因。
El-Geassy等人研究了800 ~ 1100℃温度下H2/CO气体混合物中氧化铁的还原行为[28]。他们证明,反应机制受到成型煤的原始结构(特别是孔隙度和晶粒尺寸)和气体组成的高度影响。在初始阶段,用氢气还原致密型煤时,还原反应是化学控制的。当使用CO或CO/H2混合物进行还原时,还原过程受化学反应和气体扩散的联合调节,随着还原气体中CO含量的增加,气体扩散的贡献越大。
如今,全球钢铁生产面临的主要问题之一是废物的管理,包括钢铁行业各个步骤产生的磨屑、粉尘、污泥和细粒。在球团的码垛、运输和处理过程中,球团粉的产生仍然是炼钢过程中的主要挑战之一。目前,钢铁制造企业在DRI生产、电弧炉、铸造和轧制过程中产生了相当数量的含铁副产品。2020年,全世界生产的罚款数量估计约为2000万吨。利用这些废弃物是节约资源、减少污染的重要手段[29,30,31,32]。
最近,氢在全球钢铁产业和学术界都成为了焦点问题。它提供了一个可行的选择,通过优化钢铁行业中氢气和富氢资源(如天然气和生物质)的使用,可以高效地减少二氧化碳排放和炼钢中的焦炭消耗。这些解决方案需要广泛的研究,以了解和适当评估其对钢铁生产和减少二氧化碳排放的影响。了解动力学分析对氢气还原过程的研究是有益的。
尽管关于氢还原氧化铁的研究已经有很多,但由于涉及到许多变量,如还原发生的温度、还原气体的组成、氧化铁或铁矿石的组成、孔隙度、粒度等,仍然需要更好地了解反应机理。本研究的重点是在实验室实验中,在700至1000°C的温度下,使用H2-Ar气体混合物,减少DR工厂使用的工业颗粒作为废物产生的细粒。随后,对还原样品进行表征,评价不同因素对还原过程的影响,预测还原动力学和机理。
实验
原材料
本研究中使用的氧化铁球团粉是从DR工厂(埃及亚历山大的Ezz El-Dekheila钢铁公司)获得的,作为球团运输和加工过程中产生的废物。
契约准备
用6%的蒸馏水湿润氧化铁颗粒,然后用液压机在圆柱形模具中以20 kg/cm2的速度压缩相同重量的颗粒,以生产尺寸和形状相似的颗粒。形成的压实物在110°C下干燥24小时,并储存在干燥器中进行后续表征。
在1100℃条件下,用H2气体进行初步还原实验,直到样品的重量达到一定常数,以确定氧化铁球团颗粒的总可还原氧含量(wo)。(Eq. 1)然后使用Eq. 2估计时间t (Rt%)的减少程度。
(1) (2)式中,wi为样品初始质量,wf为样品最终质量,wt为样品在t时刻的质量,wo为总氧含量。
表征工具
化学成分分析采用x射线荧光法(XRF Advanced Axios, PAN analytical,荷兰)。采用x射线衍射技术(XRD, PAN Analytical Empyrean, Eindhoven, Netherlands),在40 kV和30 mA的Cu辐射(λ = 1.5Ǻ)下,对氧化铁颗粒和还原样品中的不同物相进行了鉴定。采用反射光显微镜(Zeiss Axio-scope A1)和扫描电镜(SEM) (JEOL-JSM-5410, 10 kV,日本)检测样品的形貌和微观结构。XPS分析使用美国Thermo Fisher Scientific公司的K-Alpha x射线光电子能谱仪,提供单色Al k - α x射线源。仪器在1 × 10-7 Pa的压力下工作。在200 eV的通能下获得了广泛的调查扫描,以确定矿物表面的元素组成。在通过能量为50 eV时获得了窄分辨率扫描。数据采用A vantage软件处理。
采用x射线荧光(XRF)和x射线衍射(XRD)分析了样品的化学组成和不同相。结果分别如表2和图1所示。样品中的主要相为赤铁矿(Fe2O3),约占96%。氧化铁球团颗粒粒度分布如表3所示,可以看出60%以上的样品由< 100 μm粒径范围的颗粒组成。
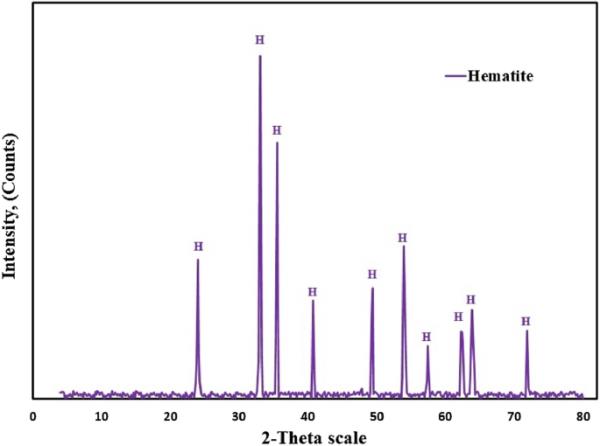
氧化铁颗粒的x射线衍射
减税制度及程序
还原系统
热重法(TG)监测样品的反应行为如图2所示。还原装置的主要组成部分包括供气系统、垂直管式炉、氧化铝反应管配件、自动灵敏天平和温度控制器。天平的输出与记录系统耦合,用于连续监测体重减轻。控制部分由两个不同的热电偶(T1和T2)组成。热电偶T1和T2分别用于测量炉温和试样温度。气体供应系统和气体净化装置用于去除气体中的水分和其他污染物。
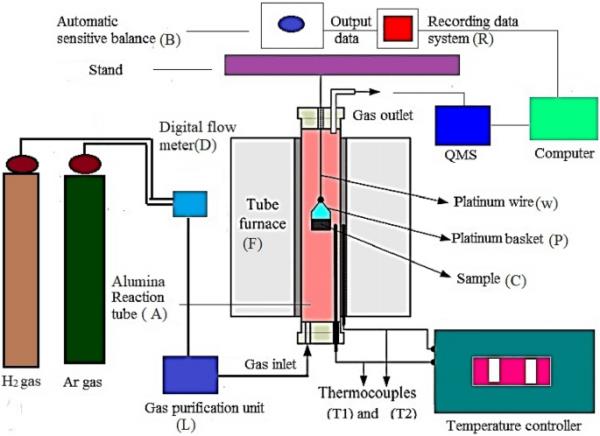
减速系统示意图
实验程序
在每个实验中,在氩气气氛中以500 ml/min的流速将致密物(氧化铁颗粒)从室温加热到目标温度,并在该温度下保持约5分钟。在此条件下,Ar被H2取代,并保持相同的Ar气体流速。在整个实验过程中,通过热重分析(TG)技术不断测量样品的失重,直到重量达到恒定值,表明实验完成。实验结束后,关闭H2气体,再次引入Ar气体,同时将炉膛冷却至室温。将还原产物取出并储存在干燥器中,以供后续分析。
目录
摘要 介绍 实验 结果与讨论 结论 参考文献 致谢 作者信息 搜索 导航 #####结果与讨论
H的作用2有限公司关于还原行为的内容
图3显示了900℃时气体成分对样品等温还原行为的影响。可以看出,随着混合气体中H2浓度的增加,还原程度和反应速率受到显著影响,这与其他研究者的实验和数值结果一致[33,34,35]。由图3可知,在纯H2的情况下,还原反应在约40 min完成,还原程度约为100%。还可以注意到,对于使用不同H2含量气体混合物得到的所有还原曲线;还原速度开始迅速并略有减速,而在还原约15分钟时,观察到还原速度明显减慢。表4显示了使用不同H2含量的还原性气体混合物进行15分钟还原后的还原程度。
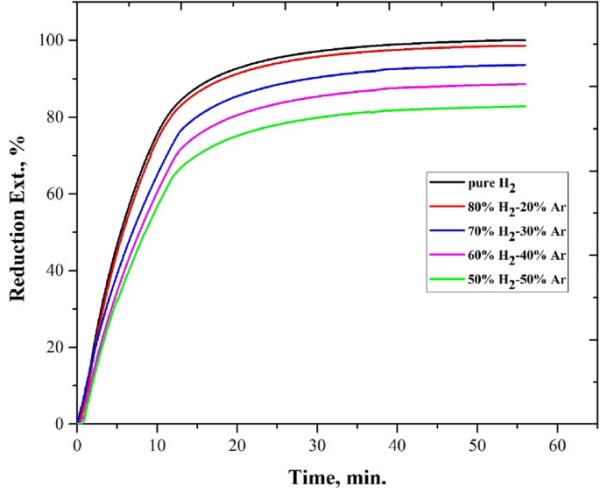
H2含量对900℃还原试样还原行为的影响
很明显,随着混合气体中H2含量的增加,达到的还原程度也随之增加。当H2含量增加80%以上时,还原程度没有明显改善。说明H2含量> 80%对还原行为没有影响。
不同样品在900℃下的还原速率与还原分数的关系如图4所示。还原率是通过还原分数作为时间函数的一阶导数来计算的。还原反应可分为三个不同的阶段。在第1阶段,虚线表示还原分数约为0.11,代表理论上预期的赤铁矿到磁铁矿的还原。第II阶段标志着磁铁矿向浮氏体的还原,还原分数约为0.33。最后,第三阶段为浮氏体向金属铁的转变。在第一阶段,还原速率最高,达到30 mg/min左右。第二阶段还原速率变小,随着混合气中H2比例的增加还原速率增大。第三阶段的还原速率是其他两个阶段中最低的,随着还原分数的增加,还原速率逐渐变缓。其它温度下的还原行为与900℃时的相似。
900℃时H2-Ar混合物还原压坯的还原速率与还原分数
温度对还原行为的影响
在700 ~ 1000℃范围内,80% H2-20% Ar混合气体还原试样的还原曲线如图5所示。考虑每条曲线;还原速率在初始阶段最大,随着反应的进行逐渐降低。在初始阶段,计算的还原程度更加明显,直至特定水平,这取决于所采用的温度。在最后阶段,除氧速率极慢,还原速率显著降低,直到还原反应完成,形成平台形状。低温时反应时间较长,而还原时间随温度升高而缩短。此外,随着温度的升高,高原的还原程度也在增加。初期和中期的高还原速率是由Fe2O3先还原为Fe3O4,再还原为FeO引起的。在最后阶段,由于FeO转化为Fe,还原速率减慢。
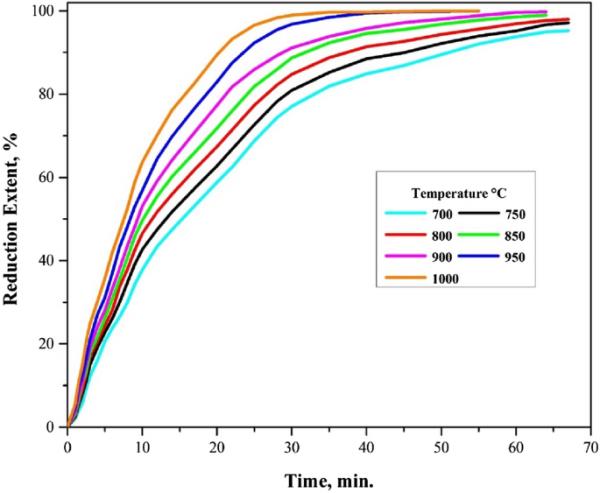
80% H2-20% Ar混合气体在700 ~ 1000℃下的还原行为
还原动力学及机理
以往的研究[5]表明,氧化铁的还原应该从表面开始,向核心发展,随着时间的推移,未反应的核心直径减小,直到为零。还原动力学可以用一个收缩的、未反应的核模型来表示,以解释还原过程。最初的假设是铁矿颗粒完全由赤铁矿组成。随着还原的进行,形成铁层,未反应的球团颗粒的核心直径缩小。铁矿石颗粒表面有一层反应物气体。外扩散、内扩散和化学反应是还原反应的三个步骤。
- 1.
反应物气体组分从主气相通过气界向球团表面扩散,称为外扩散。
- 2.
气体组分通过物理、化学方法吸附在球团表面,向反应前界面扩散,称为内扩散。
- 3.
气体组分在前界面与球团发生化学反应,生成气体氧化产物。
- 4.
气体氧化产物扩散回球团表面(内部扩散),并通过气体边界转移到主气相(外部扩散)。
为了预测铁矿石还原气固化学反应的极限机理,将数学模型与实验结果进行对比,并与表观活化能值和样品的形态特征进行关联[36,37,38]。化学反应用Arrhenius方程表示,如式(3)所示:
(3)式中,K为反应速率常数,A为指前因子,Ea为表观活化能,R为气体常数,T为绝对温度。
反应速率(K)由图5所示的还原曲线得到。link和(1/T)之间的相关性显示在反应的早期、中期和最后阶段,如图6所示。初期、中期和后期的Ea值分别为16.36、29.24和49.35 kJ/mol。
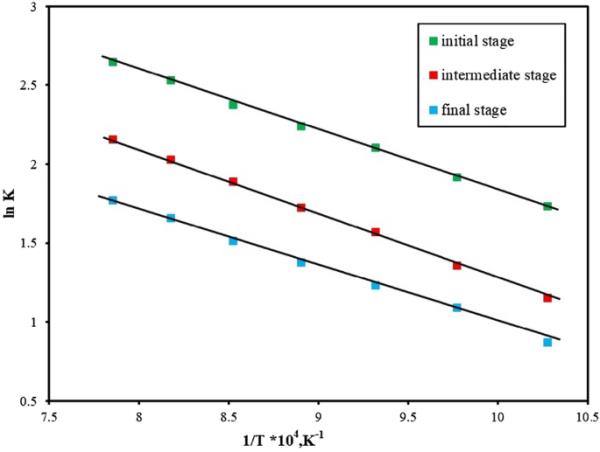
样品的Arrhenius图降低了80%H2-20% Ar
早期的Ea值表明还原反应似乎是化学反应控制,而后期的Ea值表明气体扩散是限制机制。在中间阶段,还原过程受气体扩散和化学反应的混合机制控制。其他研究在还原实验中也发现了类似的结果[39,40]。
Szekely等人[39]提出的颗粒模型是经常用于推断气固化学反应动力学和机理的数学方程之一。通过对气体扩散、化学反应和混合控制的数学公式的检验,确定了整个还原反应的速率控制步骤。以下是三个数学方程[39,40,41]:
(4) (5) (6)式中,K为反应速率,X为还原分数。
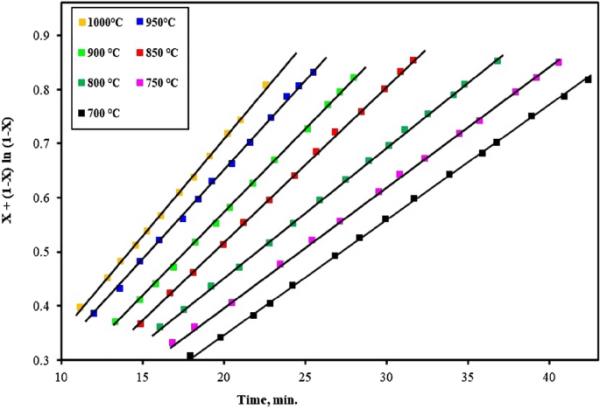
为了预测铁矿石还原气固化学反应的极限机理,将上述数学方程与实验结果进行对比,并与Ea值进行关联,验证还原机理的有效性,如图7、8、9所示。在前期对化学反应式进行测试时,观察到如图7所示的线性相关性。在中间阶段,使用如图8所示的混合控制机制实现了线性相关性。在最后阶段,通过应用如图9所示的气体扩散机制获得线性相关性。这与Ea值提出的机制相匹配。
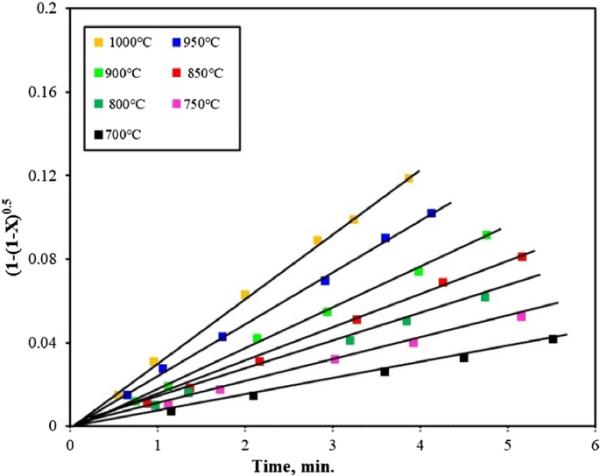
80%H2-20% Ar还原初期机理控制数学公式的应用
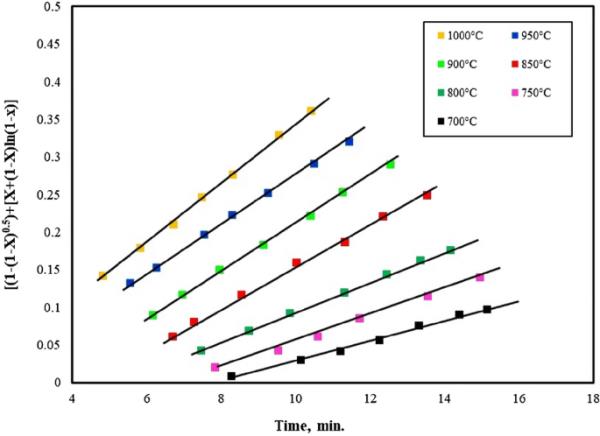
80%H2-20%还原中间阶段机理控制数学公式的应用

80%H2-20% Ar还原最后阶段机理控制数学公式的应用
为了研究还原机理,选择900℃等温还原温度,在不同还原程度中断还原反应;10,25,50,75和100%。根据60min后得到的最大质量损失来计算还原程度。将中断还原的样品在Ar气氛中冷却到室温,以终止反应过程并防止氧化。通过XRD和XPS对还原样品进行表征,确定了还原过程中的相变,并通过光学显微镜和SEM-EDS观察了其微观结构的演变。
不同样品部分还原模式的XRD谱图如图10所示。还原反应开始时,还原幅度达到10%和25%后,样品中明显以赤铁矿和磁铁矿为主。随着还原反应的进行,还原程度达到50%,主要相为磁铁矿和浮思体。这表明赤铁矿根据反应(式7)还原为磁铁矿,而磁铁矿相后面的浮士体相的出现也是磁铁矿根据反应(式8)还原为浮士体的结果。
(7) (8)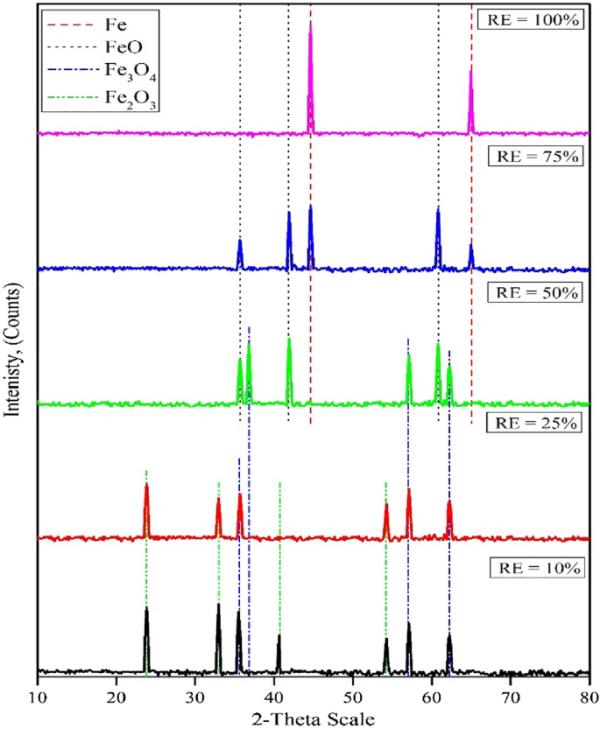
900℃下部分还原样品的XRD图谱
在75%和100%还原度的情况下,根据反应(公式8和公式9),增加还原时间可以增强磁铁矿还原为浮思体和浮思体还原为金属铁。
(9)当还原程度达到75%左右时,只检测到乌氏体和铁相。随着还原时间的延长,浮氏体相的强度逐渐降低,直至完全还原到100%,此时只检测到金属铁相。从赤铁矿到金属铁(Fe2O3-Fe3O4-FeO-Fe)的还原反应是分步进行的;这与其他研究者的研究结果一致[23,42]。
采用Rietveld精细化的XRD定量分析方法检测部分还原样品的Fe2O3、Fe3O4、FeO和Fe含量[43],见表5。结果表明,10%还原度后,相组成为82.9 wt.% Fe2O3和18.1% Fe3O4,与反应式(7)的理论转化值吻合较好。将还原度提高到50%,根据反应式(8),将还原程度提高到75%,根据反应式(9),由浮思体还原为金属铁,使还原样品的矿物组成由68.7 wt% Fe和31.3 wt% FeO丰富,还原样品中Fe3O4含量为45.1% wt.%, FeO含量为54.9 wt.%,赤铁矿完全还原为磁铁矿,产生的磁铁矿有近一半被还原为浮思体。
同时,用XPS测定了在不同还原程度下中断的还原样品的表面氧化状态,并证实了XRD所提出的还原机理。图11为不同还原度Fe的XPS谱图。不同氧化态铁的XPS峰位置;许多研究者研究了Fe+3, Fe+2, Fe0[44,45,46],根据铁的价态,这些峰的位置在706.6 ~ 711.2 eV之间。从图11可以看出,在10%还原程度下,铁的XPS峰出现在710.7 eV处,说明该样品的主要价态为赤铁矿的铁+3。此外,在719.8和732 eV处,我们还可以清晰地探测到两个赤铁矿特有的卫星峰[44]。而将还原程度提高到50%,则会促进FeO的形成,这可以通过峰从710.7 eV移到710.5 eV以及718.4和731.8 eV两个卫星峰的出现来证实[45]。进一步降低75%,峰值从710.7 eV移至710.3 eV。完整还原样品(100%)的XPS峰结合能为706.3,与零价铁(即金属铁)匹配良好[46]。
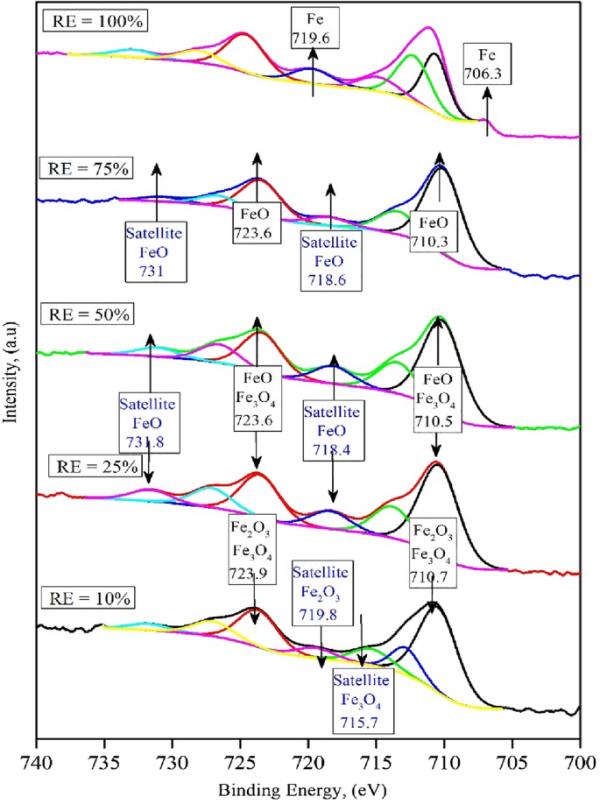
900℃下部分还原样品铁的XPS光谱
通过对不同还原程度中断还原样品的XRD和XPS相组成分析,发现还原反应是由赤铁矿逐步还原到金属铁的。(Fe2O3-Fe3O4-FeO-Fe)。
用反射光显微镜(RLM)观察900℃下部分还原样品的相变和形态特征,如图12a-f所示。图12a显示,还原以拓扑化学模式发生,形成三个不同的层(外层、中间层和核心层)。还原过程开始时,还原性气体吸附在Fe2O3表面,使其还原为Fe3O4, Fe3O4再还原为浮氏体,最后生成金属铁,由于氧的去除,形成相对多孔的结构,促进了气体扩散过程。靠近表面,气体混合扩散阻力最小,因此,化学反应阻力作为控制机制具有显著作用。图12b描绘了中间和核心层之间的一个尖锐的界面,以及致密体的外层,由铁-浮斯体相组成,扩散在浮斯体晶粒中。因此,铁在浮斯体颗粒表面成核生长,形成了铁-浮斯体共生层。随着浮氏体晶粒周围金属铁层直径的增大,对还原性气体扩散的阻力增大。结果表明,气体扩散对还原机制的贡献增大。由此可以得出,中间还原阶段的速率控制机制是化学反应和气体扩散机制的综合作用。图12c表明,外层由金属铁和具有许多大孔的浮氏体组成,使还原性气体能够很好地进入内层。还原性气体容易通过外壳扩散,使铁成核长大。随着还原过程的进行,金属铁晶粒逐渐增大并相互连接,结构中包含少量的浮氏体晶粒和金属铁,如图12d所示。随着还原时间的增加,由于金属铁晶粒之间的聚结和整合,内部结构变得更加致密,如图12e所示。这导致反应速率在最后阶段减慢,表明对气体扩散的最大阻力。因此,气体扩散控制了最后阶段的还原过程。

900°C部分还原样品的RLM显微照片,还原程度不同:a 10%, b 25%, C 50%, d 75%, e 100%
样品在900°C温度下不同时间还原的SEM图像如图13a-e所示。随着还原反应的进行,还原样品的形态结构呈现出晶粒逐渐变化的趋势。最初,内部结构表明由于氧的去除促进了气体扩散过程,形成了相对多孔的结构。XRD分析表明,中间相主要为磁铁矿。由赤铁矿还原为磁铁矿,甚至还原为浮氏体,由于晶格中氧的损失,形成了许多孔隙。随着还原反应的进行,晶粒逐渐变大,结构相对致密,孔隙减少。随着进一步的还原,金属铁(可能含有一些浮氏体)的含量增加并相互结合,形成致密的组织。这一阶段还原速率的减慢是由于形成了致密的外层,阻碍了还原气体的扩散。

900°C部分还原样品的SEM图像,还原程度不同:a 10%, b 25%, C 50%, d 75%, e 100%
结论
目前,研究人员对利用氢作为还原剂来减少钢铁行业的二氧化碳排放量很感兴趣。此外,研究还原过程的动力学机制对于确定精确的材料和能量消耗非常重要。本研究研究了DR厂使用的氧化铁球团在H2-Ar气体混合物中产生的废弃细粒的等温还原。根据实验结果,推导了还原动力学和还原机理。主要结论是:
- 1.
还原速率和还原转化率受温度的影响较大。
- 2.
在任意温度下,还原速率随H2含量的增加而增加。
- 3.
H2含量大于80%时,对还原行为没有影响。
- 4.
还原反应由Fe2O3→Fe3O4→FeO→Fe依次进行。
- 5.
前期还原过程受化学反应控制,中期还原反应受混合气体扩散和化学反应机制控制。气体扩散是后期的速率控制机制。
- 6.
计算得到的反应初期、中期和后期的表观活化能分别为16.36、29.24和49.35 kJ/mol。








