摘要
新冠肺炎后的认知缺陷,包括“脑雾”,在临床上是复杂的,既有客观因素,也有主观因素。它们很常见,使人衰弱,并可能影响工作能力,但其生物学基础尚不清楚。在这项对1837名因COVID-19住院的成年人进行的前瞻性队列研究中,我们确定了在急性入院期间测量的两种不同的生物标志物谱,可预测COVID-19后6个月和12个月的认知结果。第一种分析将纤维蛋白原相对于c反应蛋白的升高与客观和主观认知缺陷联系起来。第二种分析将相对于c反应蛋白的d -二聚体升高与主观认知缺陷和职业影响联系起来。第二种症状是由疲劳和呼吸短促引起的。这两种情况都不受抑郁或焦虑的显著调节。二次分析的结果是稳健的。在一个大规模的电子健康记录数据集中复制了它们,并测试了它们对COVID-19的特异性。这些发现为了解covid后认知缺陷的异质性生物学提供了见解。
主要
许多人在SARS-CoV-2感染1、2、3、4、5后的几周和几个月内,在隔离或急性后COVID-19综合征(也称为长COVID)期间出现神经精神症状。八分之一的患者在COVID-19后的6个月内首次接受神经或精神诊断(参考文献7)。在这些症状中,认知缺陷(包括“脑雾”)尤其令人担忧;它们是常见的、持续的,并且会影响工作能力。
covid -19后的认知缺陷如何发展仍然未知。阐明这些机制是确定潜在治疗方法和减轻COVID-19负担的关键一步。几种假说已经形成,包括内皮损伤、神经炎症、血栓形成事件、病毒入侵和低氧血症13,14,15。其中一些机制可能涉及具有持续临床表现的急性病理,而其他机制可能仅在急性期后出现13,16。最近的动物研究(17,18,19,20)和体外分析(21)正在深入了解COVID-19如何影响大脑。covid -19后尸检显示多灶性血管损伤和微血栓伴内皮细胞活化22。
其他研究已经调查了COVID-19急性期的生物学状态如何预测急性后的结果23,24,25。这些研究表明,免疫机制可能是COVID-19急性后症状的基础;然而,它们几乎没有提供关于COVID-19后认知缺陷生物学的信息,因为后者要么与其他条件合并为单个急性后COVID-19评分23,要么表示为单个自我报告的二元(是/否)变量24,25。相比之下,新冠肺炎后的认知缺陷很复杂,既有客观因素,也有主观因素,可能会也可能不会影响职业功能26。“脑雾”的这些不同维度可能是由不同的生物状态预测的,支撑它们的机制与COVID-19其他并发症的潜在机制不同。
在这里,我们使用了一项大型前瞻性纵向队列研究的数据(住院后COVID-19(磷素- covid)研究;ISCTN注册编号ISRCTN10980107),以发现COVID-19入院时测量的生物标志物与急性后认知缺陷(6个月和12个月后测量)之间的关联模式。测量了客观和主观认知缺陷以及职业影响。我们使用典型相关分析(CCA),这是一种在生物医学研究中越来越多使用的方法,用于发现变量集之间的共变模式27,28,29。通过使用来自9000多万患者的电子健康记录(EHR)数据,试图在单独的人群中重现这些发现,测试了这些发现的普遍性。
结果
共1837例患者(平均(sd)年龄57.9岁(12.4岁);36.6%的女性,57.7%的男性)属于phospv - covid队列(基线特征见表1,第一列和补充表1)。
与covid - 19后认知缺陷相关的因素
6个月时的蒙特利尔认知评估(MoCA)评分(一种测量客观认知缺陷的方法)与一系列基线特征显著相关,包括年龄、教育水平和几种合并症(图1和补充图1)。患者症状问卷(C-PSQ5、30、主观认知缺陷的测量)也与一系列基线特征相关,包括年龄和合并症(特别是精神或神经疾病和慢性疲劳综合征(CFS)/慢性疼痛/纤维肌痛;图1和补充图2)。年轻的参与者和第一语言为英语的参与者的C-PSQ明显较差,但MoCA较好。所有这些变量都作为协变量包括在随后的分析中(无论它们是否与认知结果显著相关)。
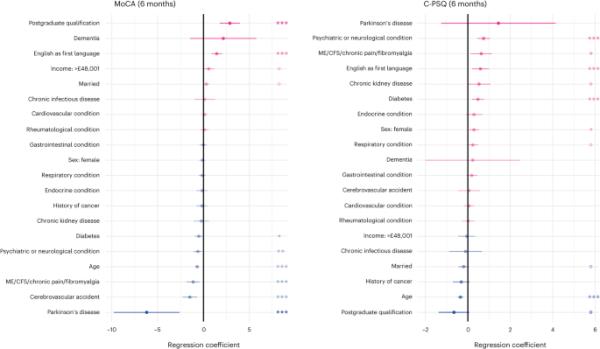
基线特征与6个月时MoCA(测量客观认知缺陷,较低表明缺陷较多)和6个月时C-PSQ(测量主观认知缺陷,较高意味着缺陷较多)之间的关联。该分析对年龄进行了z变换,这意味着该系数对应于MoCA/C-PSQ的差异,对应于1 × sd的差异。在年龄。只有一个教育水平和一个收入水平(没有教育和收入< 19,000英镑分别作为参考)。所有教育和收入水平以及种族的相同图表载于补充图1和2。N = 1837名个体参与者。点表示点估计值,水平线表示95% CI。P值作为广义线性模型的一部分进行估计,并且是双侧的,未进行多次比较调整:oP < 0.1, *P < 0.05, **P < 0.01, ***P < 0.001。国家职业资格证书。
二维l将生物标记与认知特征联系起来
CCA用于确定入院时测量的一组六种血液生物标志物(c -反应蛋白(CRP)、d -二聚体、纤维蛋白原、淋巴细胞、中性粒细胞和血小板计数)的共变异维度;这些代表了健康的各个方面,包括炎症、凝血和免疫系统反应),6个月后测量了一组14个认知得分(MoCA的7个单项和C-PSQ的7个单项)。在输入CCA之前,根据前一节中描述的所有协变量调整了所有生物标志物和认知值。每个维度由生物标记的一个线性组合(称为生物标记谱)和认知分数的一个线性组合(称为认知谱)组成,使得生物标记和认知谱高度相关。
我们确定了两个统计上显著的协变维度(r = 0.23和r = 0.17,分别为P < 0.0001和P = 0.0010),通过记录排列检验中的最大相关性来纠正多重比较;其他各维度P > 0.05)。这些维度在分裂样本分析中是稳健的,其中人群被随机分成两半100次(在第一个维度中,原始样本和分裂样本之间的权重平均相关性:生物标志物0.87,认知得分0.88;在第二个维度上,生物标记得分为0.77,认知得分为0.71;两个维度以及生物标志物和认知评分的排列检验P < 0.001)。在留一交叉验证中(r = 0.18和r = 0.11,均P < 0.0001),以及当数据仅限于完整病例时(第一个维度:r = 0.22, P < 0.0001;第2维度:r = 0.14, P = 0.008,与原维度均无显著差异(P > 0.6)。
高纤维蛋白原为1与客观和主观认知缺陷有关
生物标志物方面,第一个维度共变的特点是积极的重量为纤维蛋白原和c反应蛋白的负重量(图2)和补充表2)。这表明共变的第一个维度是由纤维蛋白原升高的CRP水平不高纤维蛋白原建议(相对于c反应蛋白升高的纤维蛋白原)考虑到这两个往往是相关群体层面上(图2)和补充表2)。在认知方面,这种共变维度是由客观和主观领域的一系列缺陷驱动的(扩展数据图1),这在COVID-19后6个月转化为显着较高的C-PSQ(主观认知缺陷)和较低的MoCA评分(客观认知缺陷)(图2b和补充表3)。这种认知特征也与12个月时显着较低的MoCA评分和显着较高的C-PSQ相关。但与职业结果的差异无关(图2b)。换句话说,入院时纤维蛋白原相对于CRP较高的个体往往在COVID-19后6个月和12个月出现客观和主观认知缺陷的迹象。
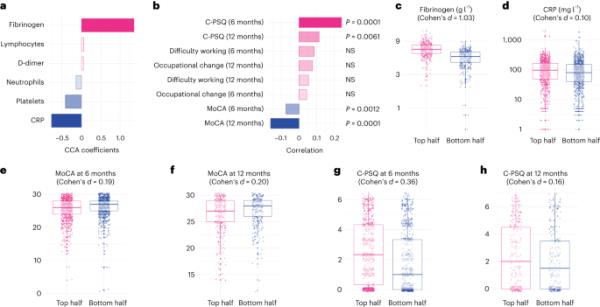
a,b,共变异的第一个维度将高纤维蛋白原和相对较低的CRP与6和12个月时较高的C-PSQ(主观认知缺陷的迹象)和6和12个月时较低的MoCA(客观认知缺陷的迹象)联系起来。P值来自排列检验,双侧检验,未对多重比较进行校正。c-h,不同变量沿第一个维度在队列上半部分和下半部分之间的分布(n分别= 768、1777、1837、626、1502和584个个体参与者)。框的中心为中位数,其边界为第25和75百分位,须的上下端为最小/最大值,距离盒图两端不超过1.5 × IQR。所有调查变量的分布见补充图4-6。Ns, p > 0.05。
通过沿着协变的第一个维度比较队列的上半部分和下半部分,可以了解该关联的效应大小。这两个亚队列具有相似的基线特征(表1,中间列)。在第一个维度的队列中,上半部分的患者比下半部分的患者纤维蛋白原水平升高(平均(95%置信区间(CI)) 6.82(6.72-6.92)比5.09 (4.99-5.20)g l−1;Cohen’s d, 1.03;图2c)和相似的CRP水平(平均(95% CI) 76.8 (71.3-82.7) vs 68.2 (63.3-73.5) mg l−1;Cohen’s d, 0.10;图2 d)。他们在6个月时的MoCA较低(25.35比26.01;平均差异0.66,95% CI 0.34-0.98;图2e)和12个月(26.22 vs 26.85;平均差异0.63,95% CI 0.13-1.12;图2f)和6个月时更高的C-PSQ (2.52 vs 1.79;平均差异0.72,95% CI 0.52 ~ 0.93;图2g)和12个月(2.27 vs 1.93;平均差异0.34,95% CI 0.0009-0.68;图2 h)。以不同程度急性后损伤为特征的预定义聚类沿该维度分布不均匀:队列上半部分的急性后损伤更严重(严重损伤的比值比(OR): 1.73, 95% CI 1.34-2.24, P < 0.0001;图2).补充图3显示了主观和客观认知缺陷与职业结果之间的相关性,补充图4-6显示了沿第一个维度在队列的上半部和下半部分开的其他变量。在6个月的随访中,第一个维度的认知特征与测量的生物标志物之间没有发现明显的关联(补充图7)。
高d二聚体是1与主观认知缺陷和职业性有关最终的结果
在生物标志物方面,共变的第二个维度是由相对于CRP的d -二聚体升高驱动的(图3a和补充表4)。在认知方面,它是由一系列跨域缺陷驱动的(扩展数据图1),这转化为显著更高的C-PSQ(更多的主观损害),但没有降低MoCA。这种认知特征也与12个月时较高的C-PSQ以及6个月和12个月时的职业结果显著相关(图3b)。换句话说,d -二聚体相对于CRP较高的个体往往在6个月和12个月时出现主观认知缺陷,以及职业影响的迹象。
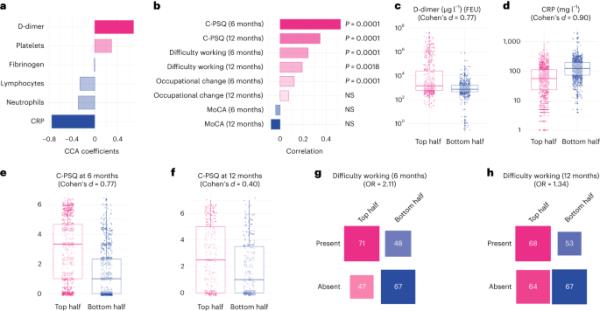
a,b,共变的第二个维度将高d -二聚体和相对较低的CRP与6和12个月时较高的C-PSQ(主观认知缺陷的迹象)和职业影响的迹象(6和12个月时受影响的工作能力和6个月时的职业变化)联系起来,但MoCA差异不大。P值来自排列检验,双侧检验,未对多重比较进行校正。c-h,不同变量在队列的上半部分和下半部分沿着这第二个维度的分布(n分别= 977、1777、1502、584、233和252个个体参与者)。框的中心为中位数,框的边界为第25百分位和第75百分位,须的下端和上端为最小/最大值,距离盒图两端不超过1.5 × IQR。所有调查变量的分布可在补充图8-10中找到。Ns, p > 0.05。
在这个维度上的上半部分的队列与下半部分的队列具有非常相似的基线特征(表1;正确的列)。与队列下半部分的患者相比,上半部分患者的d -二聚体升高(平均(95% CI) 4.97 × 103(4.06-6.07)对0.78 × 103 (0.70-0.86) μg l−1纤维蛋白原当量单位(FEU);Cohen’s d, 0.77;图3c),较低的CRP(平均(95% CI) 44.8 (41.3-48.6) vs 115.7 (109.9-121.8) mg l−1;Cohen’s d = 0.90;图3d), 6个月时C-PSQ较高(2.90 vs 1.42;平均差异1.48,95% CI 1.29-1.68;图3e)和12个月时更高的C-PSQ (2.51 vs 1.69;平均差异0.82,95% CI 0.48 ~ 1.16;图3 f)。他们更有可能在6个月时报告工作能力受损(OR = 2.11, 95% CI 1.25-3.56;图3g)和12个月(OR = 1.34, 95% CI 0.82-2.21;图3h),并在6个月时报告职业变化(OR = 1.57, 95% CI 1.21-2.05),但12个月时不报告(OR = 0.91, 95% CI 0.59-1.39)。对于第一个维度,根据预定义的聚类,上半部分的特征是急性后损伤更严重(严重损伤的OR: 2.20, 95% CI 1.70-2.87, P < 0.0001;图2).补充图8-10显示了沿第二次元划分在总体的上下半部分之间的其他变量。在6个月的随访中,没有发现第二维度的认知特征与测量的生物标志物之间存在显著关联(补充图7)。
缺席的证据新冠肺炎前的认知
如果新冠肺炎前的认知功能预测急性生物标志物特征和新冠肺炎后的认知缺陷,那么它可能会混淆所发现的关联。我们以三种不同的方式测试了这种可能性,使用了来自磷-COVID队列亚组的数据,这些数据使用C-PSQ-2 (C-PSQ项目的一个子集)报告了他们在COVID之前和6个月(n = 547)和12个月(n = 205)后的主观认知功能。
我们首先通过测试C-PSQ-2在COVID-19之前和之后是否有显着变化来评估6个月和12个月的认知缺陷是否仅仅反映了先前存在的认知缺陷。新冠肺炎后认知功能平均恶化(C-PSQ-2平均(s.e.m.)变化:新冠肺炎前至6个月0.48 (0.04),P < 0.0001,新冠肺炎前至12个月0.40 (0.055),P < 0.0001;图3)。
其次,我们评估了预先存在的认知缺陷是否能预测生物标志物特征,这将是混淆关联所必需的。预先存在的认知缺陷与两种生物标志物均无相关性(第一个维度r = 0.043, 95% CI - 0.05-0.14, P = 0.36,第二个维度r = 0.022, 95% CI - 0.071-0.12, P = 0.64)。这提供了高纤维蛋白原或相对于CRP的高d -二聚体水平在已有认知缺陷的人群中并不常见的证据。
第三,我们评估了协变的维度是否与covid前基线的认知功能变化相关。考虑到C-PSQ项目对协变维度的相对贡献(扩展数据图1),可以预期6个月时的C-PSQ-2与协变的第二个维度有关,而不是第一个维度。这被证实(C-PSQ-2与第二次协变之间的相关性:r = 0.22, 95% CI 0.12-0.31, 6个月时P = 0.0002; r = 0.20, 95% CI 0.048-0.34, 12个月时P = 0.011;与协变第一维度的相关性:r = 0.063, 95% CI -0.038-0.16, 6个月时P = 0.23; r = 0.03, 95% CI - 0.12-0.18, 12个月时P = 0.72)。因此,C-PSQ-2捕获了那些在协同变异的第二个维度上得分较高的人所经历的主观认知缺陷。我们发现,在这方面得分较高的人,认知功能的变化明显更糟(r = 0.16, 95% CI 0.061-0.26, P = 0.0021, 6个月时的变化;r = 0.27, 95% CI 0.13-0.41, P = 0.0005, 12个月时的变化)。
这些补充分析表明,生物标志物特征与主观认知缺陷之间的关联不能用covid前的认知功能来解释。
临床特征和急性疾病严重程度的调解
第一个维度捕获的关联未被14个临床量表(捕获疲劳、呼吸困难、运动耐受性、疼痛、抑郁和焦虑)显著介导,而第二个维度的生物标志物与认知特征之间的关联被呼吸困难(分数解释,8.63%,P < 0.001)和疲劳(分数解释,9.05%,P = 0.004;图4和补充表6)。
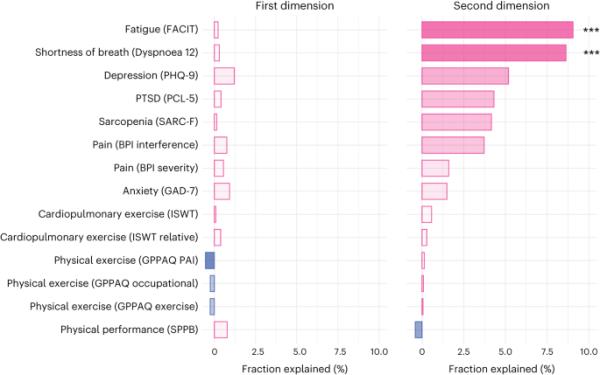
在COVID-19后6个月,通过代表健康其他方面的量表对共变第一和第二维度中捕获的关联进行调解。各比额表的名称列在括号内。P值使用重复1000次的非参数bootstrap估计,并且是双侧的,未针对多次比较进行调整:***P < 0.001。对于第二个维度,疲劳的P值为0.004,呼吸短促的P值<0.001(低于1000次重复可检测到的最小阈值)。慢性疾病治疗的功能评估;简要疼痛量表;SARC-F,肌少症筛查;增量穿梭行走试验;全科医生身体活动问卷;短物理性能电池;PHQ-9:患者健康问卷;PTSD,创伤后应激障碍;PCL-5, PTSD检查表;广泛性焦虑障碍量表GAD-7;体力活动指数。
两个维度捕获的关联没有显著介导急性疾病的严重程度(捕获一系列严重程度标记;扩展数据图4),因此当模型中包括所有介质时,它们仍然显著(第一个维度的直接效应,β = 0.26, 95% CI 0.21-0.32, P < 0.001,第二个维度,β = 0.18, 95% CI 0.11-0.24, P < 0.001)。
大规模EHR网络中的独立复制
为了评估主要发现的普遍性,我们使用一个独立且结构不同的数据集(即TriNetX分析网络)再现了分析,该数据集主要位于美国,是一个由57家医疗机构组成的EHR网络,覆盖了9000多万患者2,3。在该数据集中,确定了所有因COVID-19住院的个体,并比较了该队列中各亚组之间的COVID-19后认知缺陷风险(使用先前研究中使用的一系列ICD-10代码捕获)。对捕获COVID-19危险因素、更严重的COVID-19疾病32、COVID-19神经和精神后遗症2,3以及疫苗接种状况的82个协变量进行倾向评分匹配。
为了寻求复制共变异的第一个维度,我们比较了急性高纤维蛋白原(≥5.88 g l - 1,作为配对前人群的中位数)与急性低纤维蛋白原(<5.88 g l - 1)和正常CRP(配对后每个队列n = 1,276;补充表7描述了基线特征)。发现急性纤维蛋白原水平升高与covid后认知缺陷显著相关(在高纤维蛋白原组和低纤维蛋白原组中,6个月时的发病率分别为10.19%和6.94%;风险比(HR) 1.46, 95% CI 1.06 ~ 2.02, P = 0.019;图5)。当CRP最高水平增加一倍时,得到了类似的结果,但当CRP没有限制时,则没有得到类似的结果(扩展数据图5)。
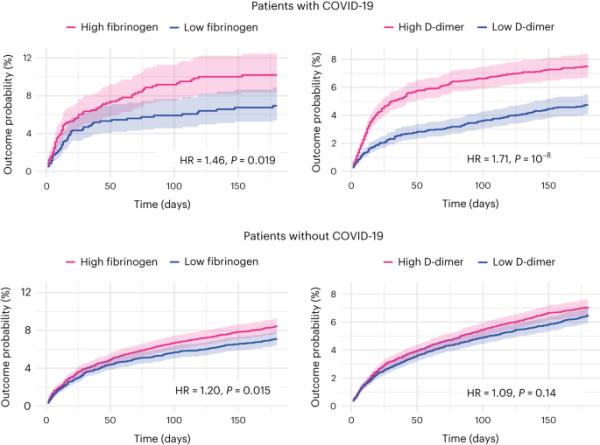
Kaplan-Meier曲线表示高纤维蛋白原(或d -二聚体)与低纤维蛋白原(或d -二聚体)和CRP水平≤10 mg l−1的患者之间认知缺陷的累积发生率。在没有COVID-19的人群中进行了相同的分析(下图)。曲线代表Kaplan-Meier估计,曲线周围的阴影代表95% CI。P值来自对数秩检验,是双侧的,没有针对多重比较进行调整。在COVID-19队列中,CRP标准放宽至包括所有CRP≤20mg l−1或完全删除的患者的相同数据见扩展数据图5。
为了寻求复制共变异的第二个维度,我们比较了匹配前急性高d -二聚体(≥14,700 μg l - 1 (FEU),作为人群的中位数)与急性低d -二聚体(<14,700 μg l - 1 (FEU))和正常CRP(匹配后每个队列n = 5,722)的患者;补充表8显示了基线特征)。发现d -二聚体水平与covid后认知缺陷显著相关(高d -二聚体和低d -二聚体队列6个月时的发病率分别为7.51%和4.74%;Hr 1.71, 95% ci 1.42-2.07, p < 0.0001;图5)。当CRP最高水平增加一倍(与主要发现一致)和CRP没有限制时,与主要发现不同,得到了类似的结果(扩展数据图5)。
在没有COVID-19的情况下,生物标志物和认知特征
为了评估生物标志物与急性后认知缺陷之间的关联是否会发生在其他疾病中,我们在一个大流行前的个体队列(没有COVID-19)中根据上述电子病历数据重复了分析。
在没有COVID-19的个体中,高纤维蛋白原与低纤维蛋白原与急性后认知缺陷之间的关联得到了重复(配对后,每个队列n = 6,782;HR 1.20, 95% CI 1.04 ~ 1.39, P = 0.015,图5;补充表9显示了基线特征),并且与COVID-19患者的风险相比,COVID-19状态没有显著降低风险(相互作用比1.23,95% CI 0.87-1.75, P = 0.25)。
相比之下,在没有COVID-19的个体中,高d -二聚体与低d -二聚体与急性后认知缺陷之间的关联不显著(配对后每个队列n = 11129;HR 1.09, 95% CI 0.97-1.23, P = 0.14,图5;补充表10显示了基线特征),并且这种关联与COVID-19状态有显著的缓和(相互作用比1.57,95% CI 1.26-1.96, P < 0.0001)。我们在事后分析中进一步探讨了COVID-19状态的这种调节作用;与d -二聚体升高但没有COVID-19的匹配队列相比,患有COVID-19和d -二聚体升高的个体在30 d时静脉血栓栓塞(VTE)的风险更高(HR 1.48, 95% CI 1.11-1.98, P = 0.007),但没有缺血性卒中(HR 0.84, 95% CI 0.50 - 1.39, P = 0.50)(扩展数据图6)。
换句话说,无论是否感染COVID-19,纤维蛋白原高的个体急性后认知缺陷的风险都增加。相比之下,高d -二聚体仅与COVID-19患者的急性后认知缺陷有关,他们与其他高d -二聚体患者的外周(VTE)血栓形成风险不同,而不是中央(缺血性中风)血栓形成风险。
目录
摘要 主要 结果 讨论 方法 数据可用性 代码的可用性 参考文献 致谢 作者信息 道德声明 同行评审 扩展数据 补充信息 搜索 导航 #####讨论
这项前瞻性队列研究纳入了1837名因COVID-19住院的患者,并对电子病历数据进行了单独的回顾性队列研究,揭示了急性血液生物标志物与急性后认知缺陷之间的两个不同维度。第一个维度将高纤维蛋白原(相对于CRP)与感染后6个月和12个月的客观和主观认知缺陷联系起来。第二个维度将高d -二聚体(相对于CRP)与主观认知缺陷以及感染后6个月和12个月的职业影响联系起来。后一种关联部分由6个月时的呼吸短促和疲劳介导。这两个维度在二次分析中是稳健的,并且在单独的大规模电子病历分析中得到了广泛的重复,这也表明与d -二聚体的关联是COVID-19特异性的,而与纤维蛋白原的关联不同。
与单变量回归相比,在单变量回归中,估计单个生物标志物和认知结果之间的协变,CCA可以捕获生物标志物和认知概况之间更复杂的关联。特别是,纤维蛋白原(或d -二聚体)和认知结果之间的单变量回归并没有揭示出显著的关联,因为它们未能捕捉到CRP在每个生物标志物谱中的重要作用(补充说明1)。与聚类不同,协变的维度并非相互排斥,因此个体可以在多个维度上获得高分。例如,纤维蛋白原和相对于CRP的d -二聚体较高的人往往在这两个方面都得分较高,并且在客观和主观认知缺陷和职业影响方面的风险更高。
结果除具有统计学意义和稳健性外,也具有临床意义。在第一个维度的队列中,上半部分的个体在6个月时的平均C-PSQ为2.52(总分7分),而下半部分的个体为1.79。这种差异可能会发生,例如,在记忆/集中注意力和理解/被理解方面,报告一些困难的人与报告很多困难的人之间。同样,在第二维度的队列中,上半部分的个体在6个月时的平均C-PSQ为2.90,平均报告了40%的主观认知缺陷症状(而下半部分的个体则为1.42或20%)。在第二维度处于上半部分的人群中,改变职业的绝对风险增加6.8%(22.1%对15.3%),报告工作困难的绝对风险增加18.5%(60.2%对41.7%)。MoCA得分在第一个维度上的差异显著,但更为温和;这可能在一定程度上反映了MoCA在检测covid后脑雾方面缺乏敏感性(而不是轻度认知障碍,它已被证实)。
这种关联是在急性期(而不是急性期后)测量的生物标志物所特有的,不能简单地用更严重的疾病(因为没有急性疾病的严重程度作为中介)或预先存在的认知缺陷来解释。多种机制可能解释了COVID-19急性期纤维蛋白原升高如何与随后的认知缺陷相关。纤维蛋白原既是炎症(作为急性期蛋白34)和高凝状态的标志。它在高纤维蛋白原水平导致更快的纤维蛋白形成和更高的纤维蛋白密度、强度和稳定性的凝血中起核心作用36。已知COVID-19可诱导高凝状态,并与纤维蛋白原升高37,38相关。也有人认为纤维蛋白原可能直接影响大脑,因为其独特的结构含有神经系统中表达的几种受体的结合位点,这可能导致小胶质细胞激活,轴突损伤和淀粉样蛋白-β39的结合。纤维蛋白原水平升高而CRP未升高与认知缺陷和随后的痴呆相关。纤维蛋白原只有在血脑屏障受损的情况下才能到达脑实质,这可能是由于SARS-CoV-2主要蛋白酶(Mpro)诱导脑内皮细胞死亡17或纤维蛋白原本身通过直接作用于这些细胞39造成的(这与纤维蛋白原升高但未感染COVID-19的患者的研究结果的复制一致)。与CRP相比,纤维蛋白原升高仅与急性后认知缺陷有关。这可能支持这样的假设,即这种生物标志物谱是由高凝血病引起的,而不是急性期反应。另一种可能性是,相对于CRP,纤维蛋白原升高代表了感染发病延迟到医院就诊,因为在CRP达到峰值后,纤维蛋白原仍然升高34。延迟呈现可能会对健康造成有害的后果,容易导致认知缺陷。为了区分这些可能性,在COVID-19急性期重复测量生物标志物的研究将提供信息。综上所述,我们关于共变的第一个维度的发现可能反映了高凝状态和纤维蛋白原对大脑的直接影响的结合。
d -二聚体水平升高在COVID-19住院期间很常见(参考文献)。35、42)。它可能有不同的原因43,但远高于正常限度的水平(如在队列中沿第二维的上半部分观察到的个体)通常表明血栓的存在44。因此,d -二聚体升高与认知缺陷之间的联系可能反映了脑血管系统中微血栓的存在,这在covid -19后的尸检中已经观察到(参考文献22),并且往往表现为d -二聚体升高和CRP45适度升高。但它也可能反映了肺血管的血栓栓塞。这一点得到了呼吸短促的中介作用的支持,并且在EHR数据中观察到,与COVID-19相关的d -二聚体升高与没有COVID-19时的d -二聚体升高在静脉血栓栓塞和急性后认知功能障碍的风险方面不同,但在缺血性卒中方面没有差异。此外,d -二聚体升高与COVID-19住院患者肺灌注减少相关(文献46),静脉血栓栓塞被认为与d -二聚体升高但纤维蛋白原47正常相关,这可以解释为什么这一机制被单独的共变维度捕获。covid -19引发的肺栓塞(pe)可能导致脑缺氧,进而导致轻微程度的认知障碍,这在主观上很明显,但不容易客观衡量(因为主观认知缺陷可能是早期衰退的敏感迹象)。体育运动与认知缺陷之间的联系的另一种解释是,体育运动可导致疲劳,而在缺乏客观缺陷迹象的情况下,疲劳可导致主观认知障碍。这被d -二聚体和认知缺陷之间的疲劳调解所支持。总之,d -二聚体升高与主观认知缺陷之间的关联可能是由covid -19相关凝血功能障碍引起的脑微血栓或pe伴缺氧或疲劳引起的。主观后冠状病毒认知缺陷与血液生物标志物相关的事实,可能对一些报告脑雾的患者是有效的,并强调了临床医生避免在没有客观迹象的情况下推断主观缺陷是微不足道的,不能有生物学基础的重要性。
这些机制的见解可能有助于进一步的研究和治疗评估。例如,对covid - 19后认知缺陷患者的脑成像调查可能会确定是否有脑缺血的证据。如果是这样,那么在高危人群急性疾病期间评估抗凝血剂可能是值得的。为了进一步测试covid - 19后认知缺陷是否可能由肺功能受损引起,肺部影像学结合纵向认知和肺功能检查将提供信息。如果这被证明是一个促进机制,那么充足的氧气支持,呼吸物理治疗和/或加强静脉血栓栓塞的预防可能会被考虑用于临床评估。此外,如果疲劳被证实是一个重要的中介,那么也可以考虑适当的职业和物理治疗支持。
除了他们提供的机制见解外,这项研究的结果可能有助于开发有covid后认知缺陷风险的患者的预测模型。这些预测模型对于告知预后、招募参与者参与旨在测试预防性干预措施的研究以及一旦干预措施可用就对其进行分层具有重要意义;然而,目前的研究尚未确定生物标志物谱的预测价值。这将需要一种不同的分析方法,在更异质的人群中复制研究结果,与其他预测因素相结合,并推导出一个经过验证的预测规则。
本研究有其优势,包括纵向性质,样本量大,主观和客观认知功能的评估,几个稳健性分析和使用大型电子病历数据库的研究结果的复制(和扩展);然而,它也有局限性。首先,该队列是在大流行早期招募的,当时还没有出现许多变体。通过使用EHR数据(不限于特定的变体)进行复制,可以部分缓解这一问题。其次,前瞻性队列研究的参与者都未接种疫苗。第三,这项研究是观察性的,不应该进行因果推理。虽然前瞻性队列研究和基于电子病历的回顾性分析都对一系列协变量进行了很好的调整,但不能排除残留的混杂因素。第四,队列研究仅限于住院患者,研究结果可能不适用于不需要住院但可能仍有认知缺陷风险的患者。第五,我们使用了一种实用的方法来定义主观认知障碍,该方法基于磷- covid研究中的可用数据(包括七个自评项目;方法)而不是经过验证的量表。第六,本研究不能区分急性疾病后持续存在的认知缺陷与初次恢复后出现的认知缺陷。虽然这两种时间线都符合较长的COVID表现,但它们可能具有不同的致病机制,本研究无法区分。第七,在大规模电子病历数据集中复制结果有其局限性(1)客观和主观认知缺陷不能分开调查;(2)生物标志物概况的比较只能通过创建和比较队列来实现,而不是评估整个范围的值。
总之,这项前瞻性队列研究发现了两个不同的维度,将COVID-19住院患者的急性血液生物标志物特征与急性后认知特征联系起来。第一个维度将相对于CRP的纤维蛋白原升高与客观和主观认知缺陷联系起来,并可能反映纤维蛋白原对大脑的潜在直接影响的免疫血栓形成事件。第二个维度将d -二聚体相对于CRP的升高与主观而非客观的认知缺陷和职业影响联系起来。该维度可能反映与covid -19相关的凝血病,伴有脑或肺血管血栓。机制是推测性的,需要进一步的研究来更好地描述它们。与此同时,这些基于常规血液检测的生物标志物谱可能有助于开发covid后认知缺陷的预测模型,从而促进预后并加速研究管理策略。
方法
PHOSP-COVID研究
对于我们的主要分析,我们使用了住院后COVID-19研究(磷光- covid)的数据,这是一项大规模的长期研究,对英国83个国家卫生服务(NHS)信托机构之一的6134名成人(年龄≥18岁)出院,临床诊断为COVID-19(2020年1月29日至2021年11月20日)5,30。在我们的分析中,我们将数据集限制为“2级”参与者(n = 2542),他们在常规临床护理的同时接受了额外的特定研究访问。第2层涉及三个时间点的数据收集:基线(住院期间)、出院后2 - 7个月(相当于入院后约6个月的平均时间,为简便起见,我们称之为6个月随访)和出院后12个月(针对一部分参与者)。收集的测量数据包括入院时的常规临床数据、入院时和随访时的血液检查结果,以及生活方式、人口统计学和临床量表。研究小组从每个地点的医院记录中获得了患者的人口统计数据和急性COVID-19入院的特征,包括对COVID-19诊断的确认、接受的治疗和器官支持。在这项研究中,我们关注的是那些在医院做过血液检查并在6个月时完成MoCA的人,这样我们的分析中每个参与者都可以获得MoCA。
关于这项研究的更多细节可以在其他论文5、16、30中找到,相关变量描述如下。所有研究参与者均获得书面知情同意。该研究已获得利兹西部研究伦理委员会(20/YH/0225)的批准,并已在ISRCTN登记处注册(ISRCTN10980107)。
生物标志物概要文件
在入院期间收集参与者的血液样本。当抽取多个血液样本时,使用入院时的第一个血样。从该样本中,提取了以下六个实验室测量值:CRP, d -二聚体(如果以d -二聚体为单位,则转换为FEU单位),纤维蛋白原,淋巴细胞,中性粒细胞和血小板。虽然本研究的重点是入院时测量的生物标志物,但在6个月的随访中也获得了相同的实验室测量值,并在事后分析中评估了它们与认知概况的关联。补充说明2提供了生物标记物谱质量控制的描述。
认知概要文件
在6个月的访问和(对于一部分参与者)12个月的访问中,对参与者的临床获得性和患者报告的临床量表进行了测量。本研究的重点是在两个维度上的认知测量:
-
MoCA可以客观地测量七个领域的认知缺陷:视觉空间和执行功能、命名、注意力、语言、抽象、延迟回忆和定向。将各个领域的得分相加,总分最高为30分,分界点为26分,通常被用作痴呆症的筛查工具51。
-
C-PSQ,根据自我报告的七个领域的损害来评估主观认知缺陷:混乱、短期记忆丧失、沟通困难、理解或被理解困难、集中注意力困难、思维迟缓和记忆困难(补充说明3包含每个项目的定义)。
对于客观和主观认知缺陷量表,单个领域的分数被用作CCA的输入(见下文)。
Occupatio最终影响
在6个月和12个月时,使用两个变量捕获了一部分参与者的职业影响。第一个变量是对一个简单问题的回答:“你的疾病是否影响了你的日常工作能力?”,我们把对这个问题有肯定回答的人称为“工作困难”。第二个变量捕获了职业的变化,并基于参与者报告他们的职业在他们感染COVID-19之前和之后发生了变化。一部分参与者还报告了他们在COVID-19之前和之后的职业。我们只记录了那些报告职业发生变化并且在COVID-19之后的职业不是“全职工作”的人的积极结果(因为职业的变化也可以反映工作时间的增加)。同样,对于报告职业变化且在COVID-19疾病前后没有职业信息的参与者,我们将职业变化报告为“未知”。
协变量
以下诊断(在诊断为COVID-19之前)和社会人口因素作为协变量纳入分析:
-
呼吸道条件
-
风湿病的条件
-
心血管状况
-
肠胃状况
-
脑血管意外
-
痴呆
-
帕金森病
-
精神或神经疾病,由对以下任何一项回答“是”的参与者捕获:(1)抑郁或焦虑;(2)抗抑郁药物治疗;(3)精神卫生专业人员的治疗;(四)其他慢性神经系统疾病
-
慢性疲劳综合症,纤维肌痛或慢性疼痛
-
糖尿病
-
甲状腺功能减退/甲状腺功能亢进或其他慢性代谢/内分泌紊乱
-
慢性肾病
-
癌症
-
慢性传染病
-
教育水平(完成的最高水平)编码为分类变量,分为以下八类:(1)无;(2)小学;(3)中学学历(GCSE水平、NVQ水平1/2或同等学历);(4)高中(a -level, NVQ level 3或同等学历);(5)职业资格(NVQ四级或同等);(6)大学本科学历或国家职业资格五级或同等学历;(七)研究生学历;(8)宁愿不说
-
家庭年收入编码为以下类别的分类变量:(1)< 19,000英镑;(2)£19001 - 26000;(3)£26001 - 35000;(4)£35001 - 48000;(5) >£48001;(6)宁愿不说
-
用一个二元变量编码的婚姻状况(已婚与未婚)
-
英语是否是参与者的第一语言,由患者报告并编码为二元变量
-
性
-
种族
卡诺相关分析
CCA是一种用于在同一个体中测量的两组独立变量之间寻找线性关系的方法。在我们的案例中,CCA被用于发现入院时血液生物标志物(每个个体测量6个变量)与6个月随访时认知评估的14个单项(7个来自MoCA域和7个来自C-PSQ域)之间的关系。首先使用广义线性模型对以上定义的每个协变量调整6个生物标记物和14个认知得分中的每一个,并将z分数标准化调整的生物标记物和认知得分输入CCA。CCA的输出是一对线性组合:一个是血液生物标志物的线性组合(血液检测结果的加权和),另一个是认知得分的线性组合(认知项目的加权和),因此前者与后者最大程度地相关。生物标志物的线性组合用一个数字总结了所有血液检测结果:具有特定血液检测结果组合的个体在该数字上得分高,而其他人得分低,从这个意义上说,我们将该线性组合称为“生物标志物概况”。这同样适用于认知项目的加权总和和由此产生的“认知概况”。
因为生物标记物和认知特征是最大程度相关的,个体可以沿着连接两者的单一维度来表示(生物标记物和认知特征之间的最佳拟合线)。我们把这个维度称为协变维度(有时也称为协变模态)。个体在这个维度上的位置可以作为他们的生物标记和认知概况的平均值来计算。
一旦发现了一个维度,并且发现它具有统计显著性(参见下一节),就可以计算它与其他未作为CCA输入的变量的相关性,从而进一步了解它所捕获的协变。根据兴趣的关联,这可以是与生物标志物概况,认知概况或平均概况(个体沿维度的位置)的相关性。在这项研究中,我们计算了每个认知概况与6个月时MoCA总分和C-PSQ总分之间的Pearson相关系数(根据上述所有协变量进行了调整),以更好地理解认知概况所代表的内容(因为它由单个MoCA和C-PSQ项目组成,而不是总分)。我们还计算了6个月时的认知概况与12个月时的MoCA和C-PSQ总分之间的相关性,以评估这种关联是否持续时间超过6个月。12个月随访时的认知项目没有被纳入CCA,以提供一个机会来测试使用6个月随访时测量的数据发现的关联是否可以预测以后时间点的结果,因为它们并非适用于所有个体。同样,我们计算了6个月和12个月时与职业结果(工作能力和职业变化)的相关性,以深入了解协变维度与职业影响之间可能存在的关联。
最后,我们还根据患者症状问卷、身体表现和认知评估数据,评估了维度是否与预定义的恢复集群(如先前基于767名磷酸- covid研究参与者子集的分析所定义的那样)显著相关。根据患者恢复的严重程度和随后的损伤程度,将患者分为四个组,分类如下:
-
轻微的损伤
-
中度损伤伴认知损伤
-
严重的损伤
-
非常严重的损伤
恢复簇变量分类编码,轻度损伤作为参考水平。
统计分析
当经Shapiro-Wilk正态性检验发现,经对数变换的变量比线性尺度变量更符合正态分布时,将血液生物标志物值转换为对数尺度。这意味着d -二聚体、中性粒细胞、血小板、CRP和淋巴细胞都是log-转化的。CCA的所有输入变量首先使用广义线性模型调整上述所有协变量,其中CCA输入(血液生物标志物或认知项目)为因变量,协变量为自变量。对于二元变量(例如C-PSQ项目的所有是/否答案)使用逻辑回归,否则使用线性回归。缺失数据(调整后的生物标志物值或认知项目)使用R (v.3.14.0)中的小鼠包,采用20条链、5次迭代的链式方程模型进行多次代入。然后将输入的数据作为CCA的输入,并使用Rubin规则将它们组合起来52。这种方法是在随机缺失的假设下使用的(即在协变量和生物标志物值的条件下,缺失的数据随机分布在参与者之间)。考虑到大量的协变量,以及本研究中所有个体的血液样本都被收集这一事实,这一假设是合理的,因此,缺失的生物标志物值代表着与方案的小偏差(例如,临床医生忘记要求部分实验室调查),而不是参与者根本没有进行血液检查。通过检查收敛图和重复整个分析(包括多次输入和CCA分析)三次并检查三次重复结果的稳定性,可以证明输入的数量(链和迭代的数量)是合理的。
为了评估共变异的维度是否具有统计学意义,应用了10,000个排列的排列检验。在每个排列中,受试者id的认知得分相对于生物标志物得分随机排列,CCA应用于结果,并记录所获得的最大相关系数(绝对值)。因此,对最大相关系数零分布的比较控制了跨协变维度的多重比较。协变维度的P值使用置换检验公式计算:
其中n = 10,000是排列的数量,n>是相关系数(绝对值)大于非排列数据集中观察到的排列的数量。
同样,为了评估外部变量(例如12个月时的职业结果或认知得分)与共变维度之间的相关性是否具有统计学意义,对外部变量的受试者id进行10,000次排列,并计算每次排列的相关系数。这导致每个感兴趣的相关系数的零分布,从中可以使用上述公式计算P值。
为了更好地理解不同变量是如何沿着协变的维度分布的,我们根据它们在该模式上的位置(沿着维度高于中位数和低于中位数)将队列划分为子组,并比较了子组之间不同变量的值。对于连续变量,原始数据以单个点表示,对于二分类变量,列联表和效应大小总结为连续变量的Cohen 's d和二分类变量的or。只有完整的(非估算的)数据以这种方式表示,以便更透明地显示可用数据(例如,这清楚地显示12个月的MoCA记录比6个月的MoCA记录少)。与恢复集群的关联以4 × 2列联表的形式报告(代表个体在四个严重集群上的分布,以及在队列的上半部分和下半部分之间沿维度),并且使用Fisher精确检验检验了处于队列的上半部分或下半部分不影响严重受损几率的原假设。
为了评估COVID-19急性期后个人健康的任何其他方面是否可能介导生物标志物和认知特征之间的关联,进行了个体中介分析,其中生物标志物特征为自变量,认知特征为因变量,个体健康的其他方面为中介。这些方面由14个临床量表编码,涵盖十个健康领域,包括呼吸短促(使用呼吸困难-12量表)、疲劳(FACIT疲劳量表)、疼痛(BPI干扰和严重程度量表)、肌肉减少症(SARC-F)、心肺运动(ISWT作为绝对得分和预测百分比)、身体活动(GPPAQ职业和运动子量表和身体活动指数)、身体表现(SPPB)、抑郁(PHQ-9)、PTSD (PCL-5)和焦虑(GAD-7量表)。对于每个中介分析,使用中介R包(v.4.5.0)对中介解释的关联部分(有时称为“间接效应”与“总效应”的比率)进行零假设检验,该零假设等于零。
为了评估生物标志物和认知特征之间的关联是否可以完全用急性疾病的严重程度来解释,我们对代表急性疾病严重程度不同方面的多个介质进行了单一的中介分析,包括:
-
世界卫生组织(世卫组织)临床进展量表53,这是世卫组织定义的一种量表,用于捕捉COVID-19患者所需的呼吸支持水平。它由四个级别组成:不需要氧气(0级);需要补充氧气(1级);需要通气(2级,我们根据住院期间任何时间点持续气道正压通气、双级无创通气或高流量鼻吸氧来获取);最后,需要进行有创通气/氧合(第3级,被捕获为有创机械通气或体外膜氧合)。这被编码为一个连续变量。
-
入院时的国家预警评分(NEWS)(入院时首次记录的NEWS)。该量表捕获了物理观察偏离其正常范围的程度,并在英国NHS全国范围内使用。它是一个范围从0到20的分数,我们将其编码为连续变量。具体来说,对不同的物理观察采用如下评分,将不同项目的得分相加得出总分:
-
呼吸频率(每分钟呼吸次数):≤8(+2分)、9-11(+1分)、12-20(0分)、21-21(+2分)、≥25(+3分);
-
氧饱和度:≤91%(+3分)、92-93%(+2分)、94-95%(+1分)、≥96%(+0分);
-
任何补充氧气:无(+0分)和有(+2分);
-
温度:≤35°C(+ 3分),35.1 -36°C(+ 1点),36.1 -38°C(+ 0分),38.1 -39°C(+ 1点),≥39.1°C(+ 2分);
-
收缩压(mm Hg):≤90(+3点)、91 ~ 100(+2点)、101 ~ 110(+1点)、111 ~ 219(+0点)、≥220(+3点);
-
心率(每分钟心跳次数):≤40(+3分)、41-50(+1分)、51-90(+0分)、91-110(+1分)、111-130(+2分)、≥131(+3分)。
-
-
住院时间:从参与者的健康记录中获取并记录为连续变量。
-
入住重症监护室:从参与者的健康记录中获取,并作为二分类变量记录。
-
入院时意识改变或意识混乱的存在:从参与者的健康记录中获取,并作为二分类变量记录。
在考虑上述介质后,连接生物标志物和认知概况的剩余“直接效应”使用lavaan软件包(v.0.6.14)针对零假设进行了测试,该假设使用z统计量来计算P值。
所有统计分析均在R v.4.2.0中进行。以双尾P < 0.05定义统计学显著性。
鲁棒性分析
结果的稳健性通过四种方式进行检验。首先进行随机分割分析,将队列随机分成两个大小相等(±1)的亚队列,每个亚队列重复分析。在每次重复中,将前两个共变维度的定义生物标志物和认知特征的系数(定义这些特征的加权和的权重)与使用Pearson相关系数(生物标志物特征的一个相关系数和认知特征的一个相关系数)的主要分析中的系数进行比较。因为CCA的定义是到配置文件的符号为止(从CCA的角度来看,将生物标志物和认知配置文件乘以- 1将是等效的结果),因此定义了符号,以便最大相关系数(绝对值)为正。由此产生的200个相关性(100次重复×两个亚队列)然后取平均值并报告。为了评估这些平均相关系数是否具有统计学意义,使用了一种排列测试,在将生物标志物值的受试者id相对于认知得分进行排列后,整个过程重复1000次(在每个排列中,生成100个随机分割的数据并计算平均相关性)。这个过程产生了一个平均相关系数的零分布,可以与初始平均相关系数进行比较,以计算P值。
其次,进行留一交叉验证。这是通过将一个参与者排除在外,并使用所有其他参与者的数据计算CCA和共变维度来实现的。然后,在所有其他参与者的基础上定义的生物标志物和认知概况被计算在被遗漏的个体中。我们在所有参与者中重复这一过程,得出每个参与者的生物标志物和认知概况,使用所有其他参与者的数据进行估计。计算了生物标志物和认知概况之间的相关系数,从而估计了前两个维度,并使用t检验检验了它等于零的零假设。
第三,数据仅限于完整的病例(排除任何生物标志物值或认知项目或协变量数据缺失的病例,n = 355),并将生物标志物和认知特征在协变的前两个维度之间的相关性与在整个队列中观察到的数据进行比较。如果在这个有限样本中相关性都显著大于零,并且与整个样本中的相关系数没有显著差异,则结果在这个完整的案例数据集中被认为是稳健的。
第四,我们评估了我们的发现是否可以归因于covid前的认知缺陷。在6个月的随访中,要求磷酸磷- covid队列中的一个大亚组(n = 547)使用C-PSQ量表的一个子集报告(回顾性)他们在感染COVID-19之前的认知功能。具体来说,他们被问到:
- 一个。
在你感染COVID-19之前,你是否有记忆困难或注意力不集中的问题?
- B。
在感染COVID-19之前,您是否有沟通困难,例如理解或被理解?
他们可以通过选择以下选项来回答这两个问题:
- 1.
否:0分
- 2.
是的,有些难度:+ 1点
- 3.
是的,难度很大:+ 2点
- 4.
是的,根本做不到:+3点
作为C-PSQ的一部分,在同一次随访期间,他们还被要求回答以下两个问题,以评估他们当前的认知功能(他们也可以从上面的四个选项中选择一个来回答):
- 1.
- C。
目前,你在记忆或集中注意力方面有困难吗?
- D。
目前,你是否在沟通上有困难,比如理解别人或被别人理解?
由于C和D是C- psq(补充说明3)中的两个项目,因此我们将它们的分数之和称为6个月时的C- psq -2,将A和B问题的答案分数之和称为covid前的C- psq -2。问题C和D在12个月后在205名参与者中重复,在12个月时提供C- psq -2。
这个纵向数据集包含了covid前和后的认知评分,使我们能够评估covid前的认知缺陷是否可以解释本研究中观察到的关联。我们首先通过测试C-PSQ-2在COVID-19之前和之后是否有显着变化来评估6个月和12个月的认知缺陷是否仅仅反映了先前存在的认知缺陷。然后,我们评估了预先存在的认知缺陷是否能预测生物标志物特征,这表明它们可能会混淆生物标志物与急性后认知特征之间的关联。最后,我们评估了6个月和12个月时的C-PSQ-2是否与共变维度相关(这很重要,因为不能保证将C-PSQ限制为两个项目编码了两个共变维度所捕获的主观认知缺陷类型),如果是这样,那么在covid前和covid后6和12个月期间C-PSQ-2的变化是否也与这些维度相关。
复制和扩展EHR数据
我们试图通过一项基于电子病历数据的回顾性队列研究来复制前瞻phospv - covid研究的结果。
研究设计和数据收集
我们使用了来自TriNetX分析网络的数据,这是一个大型联合电子病历网络,在研究时,该网络拥有来自57个医疗保健组织(主要在美国)的9000多万患者的匿名数据。在平台上收集的患者信息包括人口统计、诊断(编码为ICD-10代码)、药物和程序。使用TriNetX平台,可以根据纳入和排除标准创建队列,使用内置的倾向分数匹配算法匹配混淆变量,并在指定时间段内比较感兴趣的结果。
军团
根据以下纳入/排除标准,对两个队列进行比较,以寻求再现共变的第一和第二维度。
队列1定义为所有符合以下标准的患者:
-
(A)该个人在2020年1月20日(美国出现首例COVID-19病例的日期)当日或之后因COVID-19 (ICD-10代码U07.1)住院。
-
(B1)在因COVID-19入院前4天和入院后2周期间,个体记录的纤维蛋白原水平>5.88 g l−1(这是标准a定义的队列中的中位数)。之所以将诊断前4天内纤维蛋白原水平的患者包括在内,是因为4天被认为是获得新冠病毒检测结果的最长时间。
-
(C)个体记录的CRP水平≤10 mg l−1。纳入这一标准的原因是,共变的第一个维度发现纤维蛋白原升高并不伴随着相应的CRP升高(尽管两者在队列水平上存在相关性)。正如在结果中所讨论的,这类似于调整CRP水平。在TriNetX中调整暴露后变量(如CRP)只能通过限制队列在特定范围内的值来实现。
-
(D)个体在分析时还活着。
-
队列2、3和4被定义为符合上述标准A、C和D,但标准B1分别被B2、B3和B4取代:
-
(B2)患者因COVID-19入院前4天至入院后2周记录的纤维蛋白原水平≤5.88 g l−1。在该时间窗内,他们的纤维蛋白原水平不能大于5.88 g l−1,以避免包括在该时间窗内纤维蛋白原水平正常的队列1的患者。
-
(B3)在因COVID-19入院前4天至入院后2周期间,个体记录的d -二聚体水平>14,700 μg l−1 (FEU)(这是标准a定义的队列中的中位数)。
-
(B4)患者入院前4天至入院后2周d -二聚体水平≤14700 μg l−1 (FEU)。在该时间窗内,他们的d -二聚体水平不能超过14,700 μg l−1 (FEU),以避免包括在该时间窗内d -二聚体水平正常的队列3的患者。
为了寻求复制共变的第一个维度,将队列1与队列2进行匹配,然后进行比较。为了寻求复制共变的第二个维度,将队列3与队列4进行匹配,然后与之进行比较(详情见下文)。为了探讨标准C在上述队列定义中的重要性,通过将CRP的限制提高到≤20 mg l - 1的任何水平并完全取消该标准来重复分析。
最后,为了评估在没有COVID-19的情况下是否可以观察到生物标志物和认知特征之间的相同关联,另外一组4个队列被精确定义为1-4组,但标准A被A '修改:
(“)。该个人于2019年7月24日或之前住院。后一日期相当于美国第一例COVID-19病例前6个月(180天),因此所有这些人在进行生物标志物测量时或随后的6个月随访期间均未感染COVID-19。
结果是1 ' -4 '组;“队列1”与“队列2”匹配并比较,“队列3”与“队列4”匹配并比较。
结果
我们对180天的随访进行了时间-事件分析。主要结果是ICD-10代码的综合,这些代码捕获了出现“脑雾”的患者可能接收到的诊断代码范围,如我们之前的研究所定义的2,3,31,54。具体来说,使用了以下代码:F05(“已知生理状况导致的谵妄”)、F06.8(“已知生理状况导致的其他特定精神障碍”)、G93.40(“未指明的脑病”)、R40(“嗜睡、麻木和昏迷”)、R41(“涉及认知功能和意识的其他症状和体征”)或R48(“阅读障碍和其他符号功能障碍”)、F01(“血管性痴呆”)、F02(“其他疾病分类的痴呆”)、F03(“未指明的痴呆”)、G30(“阿尔茨海默病”)、G31.0(“额颞叶痴呆”)、G31.83(“路易体痴呆”)和G31.84(“轻度认知障碍”)。
在事后分析中,我们通过倾向评分匹配队列3与队列3,并比较自生物标志物测量后的前30天内首次缺血性卒中(ICD-10代码I63)和首次静脉血栓栓塞(ICD-10代码I82)的风险,探讨了COVID-19状态显著调节d -二聚体与急性后认知缺陷之间关联的可能原因。
统计分析
在每个比较中,比较的两个队列在确认或怀疑的COVID-19、更严重的COVID-19疾病或随后的COVID-19神经精神后果的危险因素上进行倾向评分匹配,包括2、3、32、55、56、57年龄、性别、种族、种族、社会经济剥夺、肥胖、糖尿病、高血压、缺血性心脏病和其他形式的心脏病、哮喘、慢性下呼吸道疾病、慢性肾脏疾病、器官移植、尼古丁依赖、其他物质使用障碍、肿瘤(良性和恶性)、血液癌、慢性肝病、中风、痴呆、类风湿关节炎、狼疮、牛皮癣、涉及免疫机制的疾病、精神障碍、情绪障碍、焦虑症、失眠、嗜睡、谵症、脑出血、帕金森病、格林-巴罗综合征、神经、神经根或神经丛疾病、肌神经结和肌肉疾病、脑炎、脑病、阅读障碍和其他象征性功能障碍、轻度认知障碍、癫痫、抽搐、COVID-19疫苗、抗抑郁药(特别是氟伏沙明)、抗精神病药(特别是氯氮平)和锂。更多关于协变量的细节,包括ICD-10代码,可以在补充说明4中找到。
匹配(1:1)采用贪婪最近邻算法,卡尺距离为0.1。对于每个特征,当队列之间的标准化平均差异<0.1时,匹配被认为是成功的(参考文献58)。倾向得分是使用逻辑回归计算的(由Python 3.7中scikit-learn包的LogisticRegression函数实现),包括上面提到的每个协变量。为了消除记录顺序的影响,在匹配前对协变量矩阵中的记录顺序进行随机化处理。
Kaplan-Meier估计用于估计每个结果的发生率,log-rank检验用于检验队列之间的差异。使用Cox比例风险模型计算95% CI的hr。
报告总结
有关研究设计的更多信息可在本文链接的自然组合报告摘要中获得。
下载原文档:https://link.springer.com/content/pdf/10.1038/s41591-023-02525-y.pdf







